法國數位醫療器材早期報銷程序(PECAN)之施行現況
法國數位醫療器材早期報銷程序(PECAN)之施行現況
劉怡
由於數位科技應用日新月益,一些歐盟成員國致力於制定數位療法醫材(Digital medical devices, DMD)的具體政策框架,以加強納保範圍和報銷路徑的監管,德、法便是已發展出整合監管和報銷路徑之法定框架的國家。
法國國家健康管理機構(The Haute Autorité de Santé, HAS)於2023年3月31日發布了一項用於數位醫療器材(Dispositifs Médicaux Numériques, DMN)報銷的監管框架,該法規的核心部分是引入「快速通道」或稱「早期報銷程序」,德國稱為「DiGA(Digitale Gesundheitsanwendungen)-Fast-Track」,法國則稱為「PECAN」(Prise en charge anticipée des dispositifs médicaux numériques)。
PECAN允許健康保險公司在沒有充分的臨床證據的情況下,提前將「用於治療目的的DMN」,以及「醫療遠距監測活動所使用的DMN」納入報銷一年,但不可申請延長。PECAN是數位醫療技術走向報銷與廣泛使用的重要過渡階段,此制度不僅推動人工智慧、遠距照護與智慧醫療監測等創新,更確保病人能提前受惠於這些具有益處的數位科技。
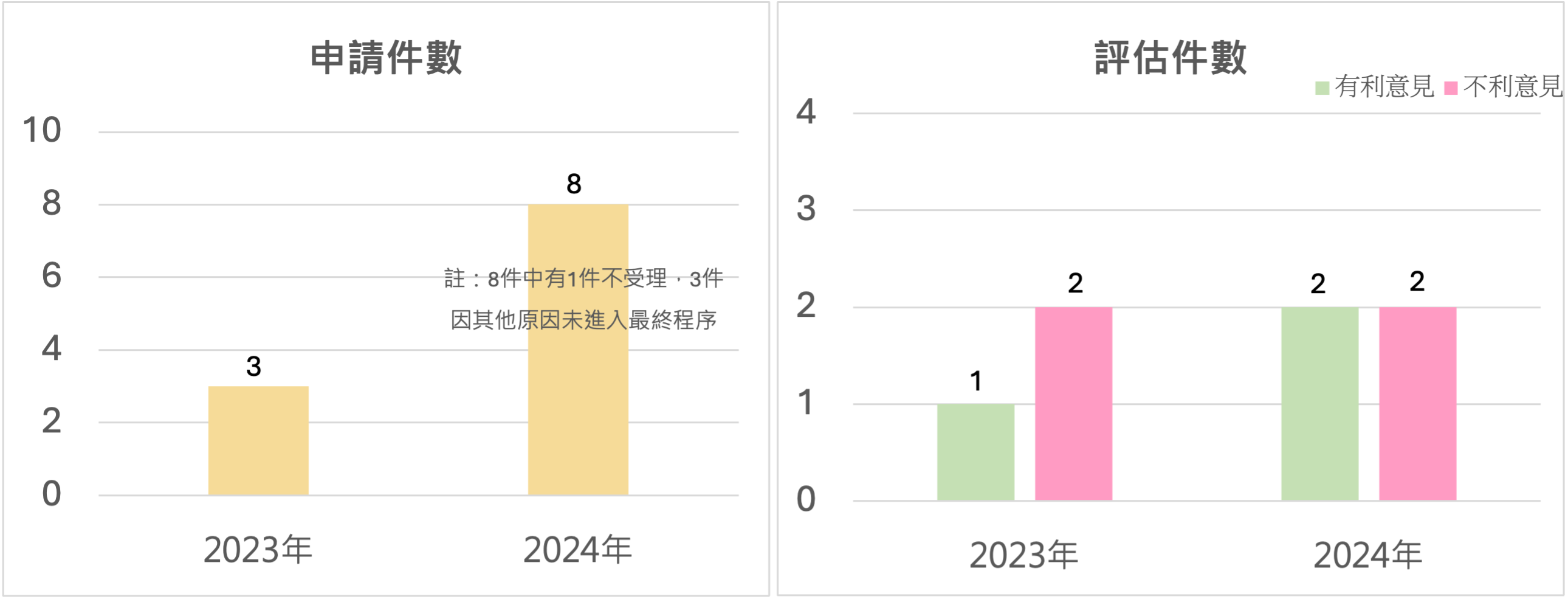
然而,相較於德國DiGA-Fast-Track已累積73件收載案件(包含47件永久收載,10件暫時收載,16件已自目錄中撤銷),法國PECAN自2023年正式施行至2024年間,HAS已收到11件的申請,其中有7件進入正式評估程序,後續獲得正向意見者僅有3件,且全部屬於遠距監測用途的DMN。目前仍尚未有任何治療用途之DMN納入PECAN早期報銷程序。
圖 1 PECAN歷年申請件數與評估件數
資料來源:資策會科法所整理自法國醫療器材與健康技術評估委員會2024年年報
PECAN評估單位—醫療器材與健康技術評估委員會(CNEDiMTS)的主席Jean-Yves Grall在其2024年出版的年報中指出,PECAN的申請數量在2024年並未如預期增加。此一現象促使評估委員會開始檢視既有機制對企業的實際適用性,並預期會進一步釐清企業在使用這些創新機制時所面臨的潛在障礙(例如資格標準、期限、研究預期及醫療需求等),以尋求更有效的方法來鼓勵創新產品開發者採用。
有鑑於此,法國HAS於2025年起啟動一系列政策研析與改革行動,包括於同年6月11日與德國簽署數位醫療器材評估合作意向書,雙方承諾兩國評估機構將透過不定期的聯合研討會,分享數位醫材報銷的評估流程、評估原則及具體案例,並承諾為規劃歐盟數位醫療器材「共同評估」框架一同努力。隨後,HAS也於2025年7月1日發布4份針對數位醫療器材報銷永久報銷與早期報銷管道的評估指引,旨在對不同報銷管道(LPPR、LATM、PECT、PECAN)的評估標準提供更具體且一致的說明。
在此次發布的數位醫療器材的早期報銷程序(PECAN)評估原則指引中,HAS說明了申請的基本資格要求,包括必須具備資料保護與互通性認證,且所考慮之適應症也需取得CE標誌。此外,指引亦再次強調PECAN評估所著重的核心面向,並列舉申請過程中常見的負面案例,旨在協助廠商在申請納入PECAN時,更能有效提升證據提交的品質。首先,該指引指出申請案件需要被推定具有創新性,也就是在「臨床效益」或「組織影響」方面展現出明確的進步,以上兩個面向的意義與具體說明列如表1。
表 1 PECAN主要評估面向
資料來源:資策會科法所整理自PECAN評估原則指引。
在申請案完成評估後,最終可能產生「有利」或「不利」兩種類型的結果,「有利」代表評估單位在審查申請者所提交的相關證據後,建議HAS將該產品納入報銷程序;相反地,「不利」則表示不建議納入PECAN。而出現「不利」結果,意味著該申請案件中,至少有一項資格標準未能符合。針對產生不利結果的常見原因,指引亦整理出幾個案例供外界參考,如表2所示。
表 2 獲得PECAN不利結果的證據提交狀況
資料來源:資策會科法所整理自PECAN評估原則指引。
觀察與結論
法國PECAN與德國DiGA-Fast-Track均為近年推動數位醫療器材早期採用的矚目政策,目的在於允許在未獲得充分的臨床證據前,即能提前納入報銷。此舉不僅期望能有效促進人工智慧與數位科技在遠距醫療與個人化醫療領域的創新發展,也使病人能提早受惠於具有潛在效益的科技產品。2023年開始推行的PECAN相較於德國DiGA-Fast-Track雖是後起之秀,但其納入DiGA-Fast-Track排除的高風險類別產品(Class III)及遠距監測類產品,顯示其政策更具開放性,也為更多具創新性的醫療科技業者提供進入早期報銷機制的機會。
然而,儘管制度看似充滿誘因,但公開資料顯示PECAN在2023-2024年間僅收到11件申請,最終獲得有利評估者更僅有3件,與法國《數位健康路線圖2023–2027》(Feuille de route du numérique en santé 2023-2027)所設定「在2026年底前達成50件PECAN申請案」的雄心目標相比,仍存在一段落差。
針對申請案件稀落的現象,有產業評論指出,主要原因可能來自高額的合規負擔、嚴格的證據門檻,以及申請者揹負著時效壓力等因素。前者包括企業需要準備大量與資料保護、互通性與醫材認證相關的證明文件,還須提出縝密的適應症設定與研究計畫書;後者指企業必須在短暫的時間內(6個月或9個月)提出充分且具意義的研究成果,才能申請轉入永久報銷。此外,PECAN不允許申請者展延為期1年的暫報銷期限。
在上述情況下,新創公司與中小型業者往往面臨沉重的前期合規成本,且在有限的時效內較難明確制定醫療院的採用模式與商業策略,因此可能有業者索性放棄此種暫時報銷的管道,寧願待獲得充分的臨床證據後逕直申請永久報銷。
面對以上狀況,法國自今(2025)年起已著手展開相關改革,包括與德國簽署評估合作意向書,並陸續發布各項評估原則指引,試圖以提升申請透明度作為改革的起點。此外,在今年11月14日於我國舉辦的醫療科技評估研討會中,HAS數位健康部的代表Corinne Collignon亦指出,HAS已與德國透過辦理研討會等方式深入探討證據門檻相關問題,並計畫未來出版一份研究報告,以更全面分析PECAN的施行狀況。故可再持續關注其政策研析成果與後續改革成效。
參考文獻
作者資訊
| 姓名 | 單位 | 職稱 | 電子信箱 | 聯絡電話 |
|
劉怡 |
資策會 科技法律研究所 |
法律研究員
|
yiliu@iii.org.tw | (02)6631-1007 |